Химиялык элементтер: аталыштары, тарыхы, таблицанын чечмелениши
"Химиялык элементтер" тууралуу кеп болмокчу. Алгач аныктамасын билип алалы. Бирдей атомдордун жыйындысы химиялык элемент деп аталат.
Жалпы маалымат
Жаратылышта кездешкен кукүрттүн бардык атомдору - күкүрт элементин, кычкылтектин атомдору - кычкылтектин элементин түзүшөт. Демек, элемент деген бир түрдөгү бүткүл атомду, ал эми атом деген сөз элементтин майда бөлүкчөсү дегенди түшүндүрөт.
Айрым химиялык атементтер - жез, алтын, күмүш, калай, коргошун, күкурт, көмүртек, цинк, мышьяк - байыркы мезгилдерде эле ачылган жана ар түрдүү элдер колдонушкан. Темирдин, сымаптын ачылыш мезгилдери биздин доорго чейин 6-2 мининчи жылдарга туура келет. XVII кылымдын биримчи жарымында Генри Кавендин суутек элементин (грек тилинен которгондо "сууну пайда кылуучу" дегенди билдирет) ачкан. 1771-жылы К. Шееле кычкылтек элементин (грек тилинен которгондо "кислотаны найда кылуучу" дегенди билдирет) ачкан. Кычкылтек 1774-жылы Пристли деген окумуштуунун тажрыйбаларында бөлүнүп алынган. 1772-жылы Д. Рутенфорд жана К. Шееле азотту (латын тилннен которгондо "туруксуз" дегенди билдирет) ачышкан.
Аталыштары
"Химиялык элементтер" ар кандай себептерге байланыштуу ат менен аталышкан. Айрым элементтер асман телолорунун аталышы боюнча аталган. Мисалы, Теллур - жердин латынча аталышы, Селен - Айдын грекче аталышы, Уран Уран планетасы, Палладий - Паллада астероиди, Церий - Церера астероиди. Айрым элементтерге окумуштуулар өз өлкөлөрүнүн атын беришкен. Мисалы, Галлий элементи - Франция мамлекетинин, Скандий элементи - Скандинавия мамлекетинин, Германий Германия мамлекетинин байыркы аталыштары, Европий - Европа материги, Эрбий Иттерби деген жердин аты, Лютеций - Париж шаарынын, Гафний -Копенгаген шаарынын байыркы аттары, Рутений Россиянын латынча аталышы.
Элементтердин кээ бир касиеттери алардын аталышын аныктаган. Мисалы, платина - күмүшкө окшош, барий - оор, фтор - бузуучу, аргон жалкоо, криптон ачылбаган, неон - жаны, ксенон - өзгөчө дегенди билдирет.
Кыскача тарыхынан
Байыркы мезгилден тартып эле XIX кылымдын жарымына чейин 63 элемент ачылган. Көптөгөн окумуштуулар ал элементтерди касиеттери боюнча катары менен жайгаштырууга аракет жасашкан. Аны биринчи жолу Петербург университетинин профессору Дмитрий Иванович Менделеев ишке ашыра алган. Бул ишти аткаруусу жөнүндө Д. И. Менделеев мындай деп жазат:
"... элементтердин массасы менен химиялык касиеттеринин ортосунда өз ара байланыш бар экендиги жөнүндөгү ой эрксизден пайда болду. Себеби заттын массасы атомдордун салмагы түрүндө туюнтулгандыктан, элементтердин өздүк касиеттери менен алардын атомдук салмактарынын ортосундагы өз ара дал келүүчүлүктү издөө керек болду. Мен ар бир элементти өзүнчө баракчаларга атомдук салмактары, негизги касиеттери, окшош элементтери жана атомдук салмактары жакын болгон элементтери менен кошо жазып алдым. Мындан элементтердин касиеттери алардын атомдук салмагына мезгилдүү көз каранды деген тыянакка келдим. Бул тыянакты чыгарууда көптөгөн түшүнбөстүктөр пайда болсо да, мен бир минута токтобостон бул чыгарылган жыйынтыкты кабылдадым."
Элементтердин мезгилдик системасы деген таблица Д. И. Менделеевдин "Химиянын негиздери" окуу китебинин биринчи басылышында (1871-жылы) жарык көргөн. Анда көптөгөн бош орундар бар болчу. Галлий, скандий жана германий элементтери ачыла элек болчу. Таблицада марганец, йод, теллур, цезий, барий, тантал сыяктуу али ачыла элек эдементтерге орун калтырылган. Көптөгөн бош орундарга (барий менен тантал элементтеринин арасында) жерде сейрек кездешүүчү элементтер туура келет. Д. И. Менделеев алдын-ала айткан элементтердин көпчүлүгү жаратылыштын өзүнөн табылган.
Азыркы учурда 118 (2016) элемент белгилүү, 94 табиятта кездешет (кээ бирлери микроэлемент катары), 24 жасалма түрдө синтезделген. Алардын айрымдарына окумуштуулардын аттары берилген. Мисалы, кюрий Мария жана Пьер Кюрилерднн урматына (1941-жылы), эйнштейний - Альберт Эйнштейндин урматына (1953-жылы), менделеевий Дмитрий Иванович Менделеевдин урматына (1955-жылы).
Мезгилдик таблица бул - Д. И. Менделеевдин мезгилдик мыйзамынын графикалык сүрөттөлүшү.

Мезгилдик таблицасынын чечмелениши
Химиялык элементтер таблицасынын чечмеленишин, жана андагы түрдүү сандар, тамгалар эмнени түшүндүрөөрүн үйрөнөбүз.
Менделеевдин таблицасынын кеңири жайылгандарына 3 форма кирет: «кыска» (кыска мезгилдүү), «узун» (узун мезгилдүү), жана эң узун. Эң узун формасында ар бир мезгил бир сапты ээлейт, узунунда деле ошол, бирок лантаноид жана актиноиддер өзүнчө таблицага жазылган, кыскасында төртүнчүдөн соңку мезгилдери эки саптка ээ. Кыска формасын мектеп окуучулары көп колдонушат. Бул макалада узун жана кыска формалары каралат, эң узун формасы каралбайт.
Мезгилдер
Мезгилдик деп аты айтып тургандай эле таблица мезгилдерге жана топторго бөлүнөт. Мезгилдер 1-сүрөттө көрсөтүлүп тургандай горизонталдык саптар менен белгиленет. Мезгилдердин саны 7, мезгилдер өз ичинен кичине жана чоң мезгилдер болуп бөлүнөт. Кичине (кичи) мезгилдерге 1-3 чейинки мезгилдер, ал эми чоң мезгилдерге 4-7 чейинки мезгилер кирет. Мезгилдердин номери атомдогу энергетикалык деңгээлдердин санын билдирет.
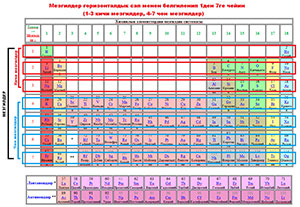
Топтор
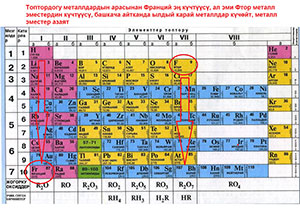
Топтор вертикалдык саптар менен бегиленип, 1ден 18ге чейин номерленет. Булар көбүнчө сандар менен жазылат (2-сүрөт).
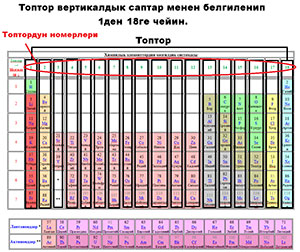
Кээде химиялык элементтердин топтору 3-сүрөттө көрсөтүлгөндөй сандык-тамга менен номерленет. Мында 3-вертикалдык саптан 12ге чейин жөн гана сан, калгандары сан жана анын жанына «А» тамгасы кошулуп жазылат. Дал ушундай жазыш керек дегенди билдирбейт, бул жөн гана белгилөөнүн бир түрү.

Меделеевдин химиялык элементтеринин мезгилдик таблицасында ушундай айырмачылыктар бар, андан тышкары таблицанын берилиши дагы абдан чоң айырмачылыктар менен берилет (4-сүрөт). Ар башка түстөр, элементтердин жайгашуусуундагы айырмачылыктар, чоң мезгилдердин өзүнчө эки сапка бөлүнүп кетиши ж.б. Эмне үчүн мындай айырмачылыктар бар? булардын кайсынысы туура? деген суроо жаралат. Бирок биз макаланын башында таблицанын 3 түрү: кыска, узун жана эң узун түрү болот деп айттык эле, ушуга байланыштуу, булар айырмаланышат.

Сүрөттө көрсөтүлгөндөй булар таблицаны түшүнүүнү оңойлатуу максатында жасалган, айрыкча ылдыйкы таблица мектеп окуучулары үчүн жакшыраак.
Топчолор (подгруппа)
Химиялык элементтер тобу негизги жана кошумча топчолордон турат. Булар «А» жана «Б» тамгалары менен белгиленип, кээде алардын ордуна сандар болушу мүмкүн, кээде эч нерсе болбошу да мүмкүн (5-сүрөт).

Негизги топчодо (подгруппада) чоң жана кичи мезгилдердин элементтери жайгашат. Кошумча топчого чоң мезгилдердин гана элементтери кирет.
Горизонталдык жана вертикалдык саптардын кесилишинде уячалар (ячейкалар) орун алып, аларда ядронун зарядынын көбөйүү иретинде элементтер жайгашат (элементтин иреттик саны деп кароого да болот). Уячанын ичинде элементтин символу, ядронун заряды (ядро заряды дайыма бүтүн санда болот), элементтин аталышы, салыштырмалуу атом массасынын саны (бул сан дайыма бөлчөктүк болот, ошондуктан тапшырмаларды аткарууда атом массасынын санын жалпылоо же бүтүндөө керек, жалгыз гана Cl-хлор элементинин атом массасы жалпыланбайт, анын массасы 35,5ге барабар) (6-сүрөт).

Элементтердин касиеттери мезгилдерде жана топтордо кандай өзгөрөт? Алгач жөнөкөй аныктамалар:
- Металл касиеттери (калыбына келүүчү) - бул атомдун электрондорду берүү мүмкүндүгү.
- Металл эместер касиеттери (кычкылдануу) - бул атомдун электрондорду алуу мүмкүндүгү.
- Электр терсдик - бул атомдун башка элементердин атомунан электрондорду тартуу мүмкүндүгү.
Элементтердин мезгилдердеги касиеттеринин өзгөрүшү
Өзгөрүү багыты солдон оңду карай.
- Мезгилде ядронун заряды чоңоёт.
- Тышкы энергетикалык деңгээлде электрондордун саны көбөйөт.
- Атомдун радиусу кичирейет.
- Металл касиеттери азаят, металл эмес касиеттери күчөйт.
- Атомдордун электр терсдиги чоңоёт.
Атомдун заряды көбөйгөн сайын, тышкы катмарда электрондордун саны көбөйүп, алардын ортосундагы тартылуу күчү чоңоет, а бул атомду кысат, ошондуктан ал кичирейет.
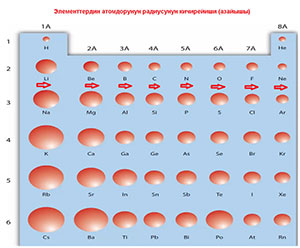
Атомдун электрондорду берүү мүмкүндүгү азаят. Башкача айтканда металл касиеттер азаят, металл эмес касиеттер тескерисинче күчөйт. Литийдин тышкы катмарында 1 электрон болсо, фтордуку 7. Ошондуктан литийге 1 электронду берүү жана фторго 1 электронду алуу пайдалуу (8-сүрөт).
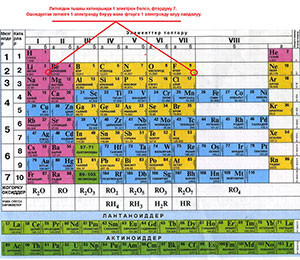
Элементтердин топтордогу касиеттеринин өзгөрүшү
- Ядронун заряды көбөйөт.
- Атомдун радиусу чоңоёт.
- Металл касиеттери күчөйт, металл эмес касиеттери азаят.
- Атомдордун электр терсдиги топтордо азаят (жогорудан ылдый карай, өйдө карай чоңоёт).
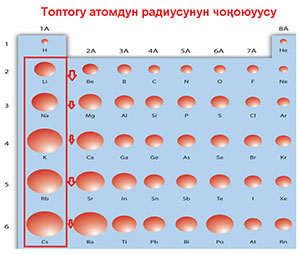
Бул жерде Фтор эң электр терс элемент.
Түстөр менен чечмелениши
Таблицадагы түстөр ар кандай болушу мүмкүн, бирок ошого карабастан түстөр химиялык элементтердин түркүмүнө тигил же бул эленттин таандык экендигин билдирет. Төмөндө таблицанын «узун» формасы түстөргө боёлуп, төмөн жагында түстөргө ылайык түркүмдөрү берилет.
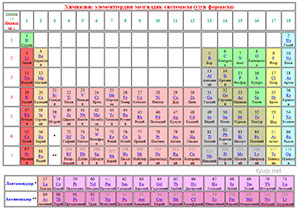
| Химиялык элементтердин түркүмдөрү | |||
|---|---|---|---|
| Жегичтүү (щелочтуу) металлдар (1-топ) | Башка металл эместер (16-топ (VI) — халькогендер) | ||
| Жегичтүү жер металлдар (2-топ) | Галогендер (17-топ) | ||
| Өтмө металлдар (3-12-топтордогулар) | Асыл газдар (18-топ) | ||
| Өтмөдөн кийинки металлдар (постөтмө) (13-16-топтор) | Лактаноиддер | ||
| Жарым металлдар — металлоиддер (13-16-топтор) | Актиноиддер | ||
Кызыктуу фактылар
- Скандий кошулган бейсбол биталары өзгөчө кубатка ээ деген имиштер бар;
- Титан элементи аллергиялык реакцияларды козгобойт ошондуктан пирсингде көп колдонулат;
- Ванадийди болотту катуураак кылуу максатында кошушат, ошондуктан ал көпчүлүк аспаптарда, ачкычтарда колдонулат;
- 50-60 жылдардагы автомобилдерди хром менен кооздошчу;
- Марганец болсо интоксикация, галлюцинация, маанайдын чукул өзгөрүүсүнө алып келиши мүмкүн;
- Темирди кимдер гана билбейт, темирди дат басат, ушул себептен буга көптөгөн башка элементтерди кошушат, эгер темирди 5000 градустан жогору ысытса ал газ сымал болуп калат;
- Кобальт дүйнөдөгү эң күчтүү магнитти жасоого жардам берет;
- Никель "шайтан жези" деп сөзмө-сөз которулат, муну көбүн эсе жашыл айнектерге кошот;
- Жез кызыл түстөгү металл, ал эң мыкты электр өткөргүч;
- Галийден жасалган кашыктар, ысык сууга салса ээрип кетет;
- Германий жарым өткөргүч болуп, биз колдонгон уюлдук телефондордо жана башка электрондук гаджеттерде көп;
- Мышьяк өтө уулу зат, ал чычкан, момолойлорго каршы дарыларда кездешет;
- Уйлар селенди көп жеп алса, шалактап, көздөрү көбөй калат;
- Бром бөлмө температурасында эле ээрип баштайт;
- Асылзат криптон газы супермен комиктеринде өтө белгилүү;
- Күмүш бактерияларга каршы эң мыкты каражат, ошондуктан аны мурда идиш-аяктарда көп колдончу;
- Суутек газ түрүндө өтө тыгыз эмес, жана суюк түрүндө планетабыздагы эң тыгыз элемент. Күндүн жарым салмагын суутек түзөт, ал эми жер кыртышындагы суутектин өлчөмү болгон 0,15%;
- Алтын көпчүлүк микрочиптерде колдонулат. 1 тонна океан суусунда 7 мгдай алтын бар. Океан сууларындагы жалпы салмагы болсо 10 миллиард тонна.
- Платинаны мурда күмүш дешчү, аны эритүү өтө татаал болгондуктан күмүштөн арзан болгон, учурда тескерисинче күмүштөн 100 эсе кымбат.
- Сымапка темирди салсаңар, темир калкып калат, барыбызга белгилүү болгондой сымап уулу зат, термометрлерде болот;
- Кадимки учактын кадимки учуусуна орточо 80 тоннадай кычкылтек керектелет. Мындай кычкылтекти 40 миң гектар токой чыгара алат;
- Жер кыртышындагы эң көп кездешүүчү элементтерге 1-орунда кычкылтек турат, анын өлчөмү 50% түзөт, андан кийин кремний 26% салмагы боюнча, үчүнчү орунда аллюминий 7%, аллюминий ушунча көп болсо неге тетиктерди дат баскан темирден жасашат?
"Химиялык элементтер" тууралуу кыргызча макала жакса же жакбаса бизге билдирип койгула.