Гальваникалык элементтер
Гальваникалык элементтер — электр тогунун туюк электр чынжырындагы эки металлдын же алардын оксидеринин электролиттеги өз ара аракеттешүүсүндө негизделген электр тогунун химиялык булагы.
Түшүндүрмөлөр
Жөнөкөй тил менен айтканда гальваникалык элемент — бул батарея. Луиджи Гальванинин атынан аталган. Химиялык энергиянын электр энергиясына өтүүсү, гальваникалык элементтерде ишке ашат.
Электрод — электр тогунун өткөргүчү, гальваникалык элементте түрдү металлдар жана графит.
Электролит — иондорго бөлүнгөн, эритиндиде жана эрүүдө пайда болгон электр тогун өткөрүүчү зат(суюктук) же катуу электролиттердин кристалл торундагы иондордун кыймылы.
Анод — оң заряддалган электрод.
Катод — терс заряддалган электрод.
Гальваникалык процесстерди изилдөөнүн тарыхы
Эки ар башка металлдардын кошулуусунда пайда болуучу электр тогунун кубулушу Италиялык физиолог, Болонья университетинин медицина профессору (Италия, Болонья шаары) Луиджи Гальвани тарабынан 1786-жылы ачылган. Галвани жез илгичтер менен байланган жаңы препарацияланган баканын арткы буттарына темир скальпелди тийгизгенде булчуңдарынын жыйрылуусун байкаган. Байкоолор Гальвани тарабынан «жаныбарлар электри» деп талкууланган.

Луиджи Гальвани
Италиялык физик жана химик Алессандро Вольта Гальванинин тажрыйбаларына кызыгып, жаңы кубулушту, тагыраак айтканда электр заряддарынын агымынын пайда болуусун байкайт. А. Вольта Гальванинин көз карашын текшерип, бир катар тажрыйбаларды жасап, булчуңдардын жыйрылуусу «жаныбарлар электри» эмес, суюктукка салынган чынжырдагы эки ар башка металлдар себепкер деген чечимге келет. Тастыктоо катарында ал баканын бутунун ордуна өзү ойлоп тапкан электрометрди коюп, бардык иш-аракеттериди кайталайт. 1800-жылы А. Вольта өзүнүн ачылыштарын биринчи жолу Лондондун Королдук коомунун жыйынында, экинчи класстагы электр өткөргүч (суюктук) ортодо эки ар башка металлдан жасалган биринчи класстагы эки өткөргүч менен байланышат, натыйжада тигил же бул багыттагы электр тогу пайда болот деп жарыялайт. Ошентип химиялык электр ток булагын А. Вольта ойлоп табат. Ал эми гальваникалык элементти Луиджи Гальвани ачкан.
1802-жылы орус физиги Василий Владимирович Петров дүйнөдөгү эң чоң гальваникалык элементти жасап чыгат, ал диаметри 35 миллиметр, калыңдыгы 2,5 мм болгон 4200 жез жана цинк тегеректерден туруп, алардын араларына нашатырь эритмесине сиңдирилген кагаз тегеректер коюлган. Петров тарабынан биринчилерден изоляция колдонулган (сургуч). Конструкция кызыл жыгачтан жасалган кутуга салынып, түрдүү чайырлардан турган изоляциялоочу катмар менен капталган. Заманбап эсептөөлөр боюнча Петровдун батареясы орточо 1500 вольт чыгарган. Орус окумуштуусу ток булагы болгон батарейканын касиеттерин изилдеп, анын аракети металлдар менен электролиттер ортосундагы химиялык процесстерге негизделгенин көрсөттү.
Электроддордун түрлөрү
Гальваникалык элементтердин курамына электроддор кирет. Электроддор төмөнкүдөй болот:
Абалына келүүчү электроддор
- 1- түрдөгү электроддор - өзүлөрүнүн туздарына чөгөрүлгөн металл электроддор;
- 2-түрдөгү - эрибеген туздар менен жалпы анионду камтыган, өзүлөрүнүн тузу менен оңой эмес ээрий турган туз эритмесине салынган металл электрод (хлор күмүштүү электрод, каломелдик электрод, металл-оксид электроддору);
- 3-түрдөгү - эрибеген эки чөкмөдөн турган элекроддор: азыраак эрий турганында металл электродунан калыптануучу катион бар, ал эми көбүрөөк эрий турганында биринчи чөкмөдөн турган жалпы анион бар;
- Газ электроддор - эритме жана газдагы терс металлдан турган электрод (кычкылтек, суутек электроддору);
- Амальгамдык - сымаптагы металлдар эритмесинен турган электроддор;
- Кычкылданып калыбына келүүчү - активдүү эмес металлдан тургандар (ферри-ферро, хингидрондук);
Ионселективдүү мембрандык электроддор
- Туруктуу зарядга ээ ион алмашуучу мембраналуу - айнек эл.;
- Суюк ассоциацияланган иониттерден турган;
- Мембрана активдүү комплексондордун негизиндеги мембранасы бар электроддор;
- Моно- жана поликрасталлдык мембраналары бар эл-дор.
Гальваникалык элементтердин мүнөздөмөсү
Гальваникалык элементтер электр кыймылдатуучу күчү (ЭКК, орусча ЭДС), сыйымдуулугу; тышкы чынжырга бере ала (берүү мүмкүндүгү) турган энергиясы; сакталуучулугу менен мүнөздөлөт.
- Гальваникалык элементтин электр кыймылдатуучу күчү электроддордун материалынан жана электролиттин курамынан көз каранды. Электр кыймылдатуучу күчү Нернст теңдемеси түрүндө жүрүп жаткан электрохимиялык процесстердин термодинамикалык функциялары менен сүрөттөлөт.
- Элементтин электр сыйымдуулугу - бул ток булагынын разряддалуусундагы берүүчү электрдин саны. Сыйымдуулук булакта сакталган реагенттердин салмагына жана алардын айлануу (конверсия) деңгээлине жараша болот; температуранын төмөндөшү же разряддалуу токтун жогорулашы менен төмөндөйт.
- Гальваникалык элементтин энергиясы сандык түрдө анын сыйымдуулугунун чыңалууну (напряжение) чыгаруусуна барабар. Элементтеги реагент заттардын санынын белгилүү бир деңгээлге чейин көбөйүүсү, температуранын көтөрүлүшү менен энергия көбөйөт. Энергияны разряддалуу токтун көбөйүүсү азайтат.
- Сакталуучулук - бул элементтин көрсөтүлгөн чектеги мүнөздөмөлөрүнүн, кайсы бир убакка чейин сакталуу мөөнөтү. Оюмду түшүнүктүү жаздым деген ойдомун :) Элементтин сактоочулугунун мөөнөтү температуранын өсүүсү менен азаят.
Гальваникалык элементтердин классификациясы
Алгачкы гальваникалык элементтер — булар химиялык энергияны, андагы реагенттерди (кычкылдантуучу жана калыбына келтирүүчү) электр энергиясына түз конверсиялоочу түзүлүш. Булактын курамындагы реагенттердин иштөөсү менен сарпталып, түгөнгөндө иш-аракети токтойт. Гальваникалык элементтин мисалы катары Даниэль-Якобинин элементин айтсак болот.
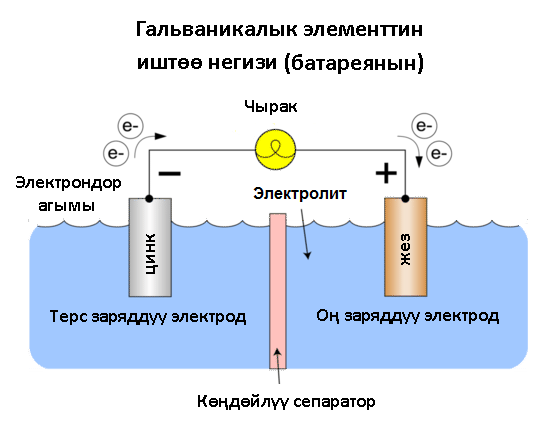
Суюк электролит эритмеси жок марганец-цинк элементтер кеңири таралган (куграк элементтер, батарейкалар). Лекланшенин туз элементтеринде цинк электроду катод, ал эми марганец диоксиди кошулган графит анод болуп, графит ток өткөргүч катары кызмат кылат. Электролит катары амоний хлорид эритмесиндеги паста, аны коюлантуу максатында ун же крахмал кошот.
Электролит катары калий гидроксидинин негизиндеги паста колдонулган жегичтүү, марганец-цинк элементтери бир катар артыкчылыктарга ээ (сыйымдуулуктун көбүрөөк болушу, төмөнкү температураларда жакшы иштөөсү жана күч келтирүүдөгү токтун жогоруулугу).
Туз жана жегичтүү элементтер радиоаппаратураларды, түрдүү электрондук түзүлүштөргө энергия берүүдө кеңири колдонулат.
Токтун кайра пайдалануу булактары (аккумуляторлор) — бул тышкы электр тогунун электр энергиясы химиялык энергияга айланып жана топтолуп (аккумуляторду кубаттандыруу), химиялык энергия болсо кайрадан электр энергиясына айлануучу түзүлүштөр.
Кеңири таралган аккумуляторлордун катарында коргошун-кислоталуу аккумуляторлор турат (автомобиль аккумуляторлору). Андагы электролит 25-30% күкүрт кислотасынын эритмеси. Электроду болсо коргошун оксиди менен толтурулган торчо сымал коргошун пластиналар, электролит менен аракеттенгенде коргошун сульфатына (II) (PbSO4) айланат.
Ошондой эле жегичтүү (шакар) аккумуляторлор да бар: Кеңири колдонууну никель-кадмийлүү жана никель-металлгибриддүү аккумуляторлор алган, электролити - калий гидроксиди (K-OH).
Түрдүү электрондук түзүлүштөрдө (уюлдук телефон, планшет, ноутбук) негизинен жогорку сыйымдуулугу жана эс тутум эффектиси жоктугу менен мүнөздөлгөн литий-иондук жана литий-полимердик аккумуляторлор колдонулат.
Электрохимиялык генераторлор (отун элементтер) — мында химиялык энергиянын электр энергиясына айлануу процесстери жүрөт. Кычкылданткыч жана калыбына келтиргичтер элементтен тышкары сакталып, иштөө учурунда электроддорго үзгүлтүксүз жана өз-өзүнчө берилет. Отун элементтеринин (топливный элемент) иштөө процессинде электроддор сарпталбайт. Калыбына келтиргич катары суутек (H2), метанол (CH3OH), метан (CH4); суюк же газ абалында пайдаланылат. Кычкылданткыч кадыресе кычкылтек болуп, абадан же таза кычкылтек берилет. Жегичтүү (шакар) электролиттүү, кычкылтек-суутектүү отун элементинде химиялык энергия электр энегиясына айланат. Энерго орнотмолор космос кемелеринде колдонулат: алар космос кемесин жана космонавттарды энергия менен камсыз кылат.
Колдонуу
Гальваникалык элементтер белги берүү системаларында, электр чырактарда, сааттарда, калькуляторлордо, аудиосистемаларда, оюнчуктарда, үналгыда, авто жабдыктарда, башкаруучу түзүлүштөрдө (пульт) пайдаланылат.
Аккумуляторлор унаалардын кыймылдаткычтарын от алдырууда, убактылуу электр энергиясы менен камсыз кылуу түзүлүштөрдө, гаджеттерде, электр жүктөгүчтөрдө, үзгүлтүксүз азыктандыруу булактарында ж. б. колдонулат.
Отун элементтери электр энергиясын чыгарууда (электр станцияларында), авариялык энергия булактарында, автономдуу электр жабууда, транспортто, алып жүрмө түзүлүштөрдө иштетилет.
Ушунун баары жалпы жонунан гальваникалык элемент болуп, дээрлик көбүнчөсү электр тогунун химиялык булагы аталат.
Жасалма элемент
Эң жөнөкөй гальваникалык элементти ар бир адам жасай алат, ал үчүн 10-15см жез зымын жана цинк пластинасын (цинктелген металлдар да болот, мисалы дат баспаган шыптардын калдыктары), чөйчөккө туздуу суу куюп, ага эки металлды салсаңыз орточо 0,5-1 вольт чыңалуу, жана 0,5-1 миллиампер ток күчүн чыгарат. Бирок мындай элемент көпкө чыдабайт, анткени суудагы туз металлдарды, өзгөчө цинкти убакыттын өтүшү менен чиритип жиберет.
Электролит катары жөнөкөй сууну колдонсо да болот, мындай учурда электроддор көпкө чейин бузулбай иштейт, бирок мындай элемент ток күчүн (ампер) абдан аз чыгарат. Көбүрөөк ток алуу үчүн электроддордун көлөмүн чоңойтуп, алардын ортосундагы аралыкты кыскартып, элементтердин санын көбөйтүү зарыл.
Биз ушундай элементти атайын текшерүү максатында жасап көрүүнү чечтик. Бийиктиги 10см, жазылыгы 5см болгон жез фольга жана цинктелген пластиналарды кесип алып, ар бир элементте бирден жез, цинк жана экөө биригип калбоосу үчүн ортосуна бийиктиги 11см, жазылыгы 6см болгон синтетикалык кездеме салдык. Бул - бир элемент болду. Ушундай элементтен 6ны жасап, ырааттуу түрдө зымдар менен туташтырдык.
Бардыгын кошкон соң, электр тогунун чыңалуусу 6 вольт, ток күчү 20 миллиамперди түздү. Буга эң жөнөкөй жарык берүү диодун кошкондо ал дароо күйдү. Мунун баары жөнөкөй суу электролитинде жасалган.

Канча убакыт иштейт экен деп, күйгүзүп койдук, 1 күн өттү өчкөн жок, 1 жума өттү өчкөн жок, болгону суусу акырындык менен буулануунун айынан азайып калды. 2 жума өткөндө суусу жок калыптыр, бирок диод дагы деле күйүп туруптур. Жаңы суу куюп койдук. Ошентип, 3 ай өттү, дагы деле тынымсыз иштеп жатат, болгону суу куюп гана коебуз. Дагы канча иштээрин билбейбиз анткени бул макаланы жазып жатканда дагы деле күйүп турган. Электродорду бири бирине тыгыз жайгаштырса ток күчү көбүрөөк болоорун байкадык.
Жалаң эле жез менен цинктен жасабастан, активдүүлүгү жогорураак металлдардан жасаса ток күчү андан дагы чоң болмокчу, мисалы, магний менен графит ж.б.у.с.
Адабияттар
- Ахметов Н. С. Жалпы жана органикалык эмес химия (орус тилинде).
- Аксенович Л. А. Орто мектептеги физика: Теория. Тапшырмалар (орус тилинде).
- Химия: 2006-жыл, ISBN 9967-426-22-5